
Říká se, že “obrázek vydá za tisíc slov” a že “vidět znamená věřit”. Pokud jde o “viry”, mají tyto obrazy podobu snímků z transmisního elektronového mikroskopu (TEM). Jsou to děsivá vyobrazení jasně zbarvených a digitálně vylepšených částic, která vidíte všude v médiích a která vás přesvědčují o tom, že nový “virus” známý jako “SARS-COV-2” skutečně existuje.
Reprezentativní částice “koróny” se opakovaně sdílí a dostává se na trička, plakáty, hračky, videohry a další.

Jak už to u nejlepších symbolů bývá, “koronavirus” se hluboce zapsal do kolektivního vědomí. Většina se neptá, zda jsou obrázky TEM, na nichž jsou tyto symboly založeny, pravé, ani jak byly vlastně získány. Lidé bezmezně věří v pravost vyobrazení těchto částic s hroty, která jim byla v posledních několika letech opakovaně v různých formách propagována.
Existuje však ještě jeden citát populárního básníka Edgara Allena Poea, který říká, že “věřte jen polovině toho, co vidíte, a ničemu z toho, co slyšíte”. Pokud jde o obrázky TEM částic, o nichž se tvrdí, že jsou “viry”, existují velmi dobré důvody, proč je zařadit do kategorie věcí, které vidíte a kterým byste rozhodně neměli věřit. Pro začátek, práce Dr. Harolda Hillmana, MB, BSc, MRCS, PhD ukázala, že většina struktur a částic viditelných na snímcích z elektronového mikroskopu jsou ve skutečnosti artefakty vzniklé při dehydrataci, vkládání, fixaci a barvení, kterými vzorky před zobrazením procházejí. Protože nic nemůže tyto procesy přežít, je vše ve vzorku v mrtvém a nepřirozeně změněném stavu. Uvádím několik citací od samotného Dr. Hillmana, který vysvětluje problémy se zobrazováním TEM:
“Jakou cenu má intelektuální poctivost?” ptá se neurobiolog
“Byl jsem natolik znepokojen myšlenkou, že subcelulární frakcionace by mohla být neuspokojivou technikou, že jsem se rozhodl vzít zcela jinou techniku a podrobit ji menší analýze. Vzal jsem si na paškál elektronovou mikroskopii a položil si otázku: ‘Kolik toho snímek pořízený tímto přístrojem vypovídá o struktuře živé buňky? Od počátku padesátých let minulého století se objevuje vášeň pro propojení “struktury” s “funkcí”, tedy vzhledu elektronovou mikroskopií identifikovatelné části buňky s biochemickými vlastnostmi, které vykazuje.
Až do 40. let 20. století se ke zkoumání živých buněk, nefixovaných tkání a obarvených řezů, používal 100 let světelný mikroskop. V té době byl zaveden elektronový mikroskop. Ten umožňuje mnohem větší rozlišení a zvětšení než světelný mikroskop, ale tkáň nemůže přežít nízký tlak, bombardování elektrony a rentgenové záření v elektronovém mikroskopu, takže musí být potažena nánosem solí osmia olova nebo wolframu, který se těmito látkami neničí, a proto může být zkoumán. Cytologové velmi toužili po tom, aby mohli tento výkonnější přístroj používat k pozorování jemné struktury buněk.”
“Například většina cytologů ví, ale čtenáři základních učebnic ne, že když se člověk podívá na ilustraci elektronového mikrofotografu: V případě, že se jedná o mikroskopický snímek, je třeba říci, že: zvíře bylo usmrceno; vychladlo; jeho tkáň se vyřízne; tkáň se fixuje (usmrtí); obarví se solí těžkého kovu; dehydratuje se zvyšující se koncentrací alkoholu; smrští se; alkohol se extrahuje tukovým rozpouštědlem, propylenoxidem; ten se nahradí epoxidovou pryskyřicí; za několik dní ztvrdne; vyříznou se řezy o tloušťce jedné desetiny milimetru nebo menší; vloží se do elektronového mikroskopu, z něhož se odčerpá téměř všechen vzduch; namíří se na něj svazek elektronů o napětí 10 000 voltů až 3 000 000 voltů; některé elektrony dopadají na fosforeskující stínítko; elektronoví mikroskopisté zvolí pole a zvětšení, které zobrazí znaky, jež chtějí demonstrovat; obraz může být zesílen; pořídí se fotografie; některé se vyberou jako důkaz. Člověk okamžitě vidí, jakou cestu ušla tkáň od života k ilustraci v knize.”
“K vlastní spokojenosti jsem ukázal, že (i) přinejmenším některé populární důležité biochemické výzkumné techniky nebyly nikdy kontrolovány, (ii) většina nových struktur v buňkách patrných při elektronové mikroskopii jsou artefakty, (iii) v mozku a míše jsou pouze nervové buňky a holá jádra v zemité látce, (iv) neexistují žádné synapse, (v) hypotéza o vysílačích je pochybná. Všechny důkazy pro tato tvrzení jsem zveřejnil, i když to nebylo vždy snadné.”
https://www.big-lies.org/harold-hillman-biology/what-price-intellectual-honesty.htm
Dr. Hillman vytvořil a publikoval důkazy, které ukazují, že procesy používané k vytvoření jakéhokoli TEM obrazu významně mění vlastnosti tkání nebo vzorků, které jsou jim podrobeny. Ukázal, že viděné struktury a částice jsou artefakty a že studie vytvářející tyto snímky postrádají nezbytné a řádné kontrolní procesy, které by prokázaly správnost jeho tvrzení. Výše uvedené stručné odstavce Dr. Hillmana nevystihují jeho práci, protože důkazy, které odhalil, značně zpochybnily přijaté vědecké dogma, že snímky TEM jsou platným důkazem čehokoli. I kdybychom práci doktora Hillmana ignorovali a stále věřili, že částice vybrané z moře miliard podobných a stejných skutečně zobrazují “viry”, existuje ještě jeden velmi pádný důvod, proč tento postoj přehodnotit.
Krize identity
Když se počátkem roku 2020 naplno rozjela mánie kolem “koronavirů”, objevily se četné studie, které údajně ukazovaly TEM snímky částic “SARS-COV-2” v různých tkáních a orgánech mimo plíce. Tyto studie byly použity k odůvodnění tvrzení, že “virus” napadá různé orgány, například ledviny. Virologové a propaganda mainstreamových médií tvrdili, že tyto snímky jsou důkazem “viru” a že lze prokázat, že se “SARS-COV-2” šíří po celém těle. Jiní vědci však začali zpochybňovat platnost snímků z těchto studií a tvrdili, že zobrazené částice nejsou “SARS-COV-2”, ale ve skutečnosti jde o jiné subcelulární vezikuly. Tito výzkumníci věděli to, co většina lidí neví, a sice že částice, o kterých se říká, že jsou “viry”, nelze odlišit od normálních “nevirových” subcelulárních částic, jako jsou všudypřítomné obalené vezikuly, například vezikuly obalené klathrinem nebo vezikuly obalené COPI či COPII, a také multivesikulární tělíska (MVB) a exozomy. Dokonce i na těchto “nevirových” částicích lze pozorovat povlak podobný koruně, který je údajně specifický pro “virus” CORONA (neboli korunu). Mnoho snímků TEM “SARS-COV-2” tak bylo právem zpochybněno.
V červenci 2020 se do této debaty vložila skupina vědců a provedla vlastní experimenty, aby zjistila, zda lze částice, o nichž se říká, že jsou “SARS-COV-2”, vybrat z mnoha podobných a stejných částic na snímcích TEM. Za tímto účelem odebrali vzorky z plic a ledvin čtyř pacientů “Covid-19”. Pomocí RT-PCR zjistili, že v plicích se nachází “virová” RNA, ale ne v ledvinách. Po ultrastrukturálním vyšetření vědci zjistili, že ve vzorcích plic s “virovou” RNA se nacházejí částice “podobné koronavirům”. Stejné však našli i ve vzorcích ledvin bez “virové” RNA. Vědci dokonce našli naprosto stejné částice “podobné koronaviru” ve vzorcích od dvou pacientů bez “SARS-COV-2”, které byly odebrány před “pandemií”. Došli k závěru, že samotný TEM není platným důkazem a že se na tyto snímky nelze spoléhat při tvrzení o “virové” invazi:
Všudypřítomné buněčné struktury nebo viry SARS-CoV-2? Aktuální dilema v éře COVID-19
“Několik zpráv naznačuje ultrastrukturální důkazy přímé infekce různých typů ledvinových buněk koronavirem těžkého akutního respiračního syndromu 2 (SARS-CoV-2) v posmrtných analýzách a vzorcích ledvinové biopsie u pacientů s prokázanou virovou reverzní transkriptázovou polymerázovou řetězovou reakcí (RT-PCR) z nosohltanových stěrů. Detekce předpokládaných virových částic transmisní elektronovou mikroskopií (TEM) byla použita jako dostatečný důkaz virové invaze do ledvinné tkáně, ale chyběly údaje týkající se detekce virové RNA nebo jiných hodnotných metod pro detekci viru ve vzorcích ledvin. Stejně tak další studie navrhovala přímou infekci endoteliálních buněk SARS-CoV-2 ve více orgánech pacientů s koronavirovým onemocněním 2019 (COVID-19) pouze na základě TEM. Prezentované částice ve výše uvedených studiích vykazují průměr 50 až 150 nm a elektronově hustý plášť podobný koruně, takže se mohou jevit jako podobné koronaviru, ale také jako podobné všudypřítomným obaleným vezikulám, jako jsou vezikuly obalené klathrinem nebo vezikuly obalené COPI či COPII. Shluky virových částic uvnitř vakuoly se navíc mohou podobat multivesikulárním tělískům (MVB), což jsou pravidelné struktury endocytické dráhy.
Za účelem zjištění přímé invaze viru SARS-CoV-2 do ledvin jsme provedli RT-PCR na čerstvých posmrtných vzorcích plic a ledvin 4 pacientů s COVID-19. Na základě těchto vzorků jsme zjistili, zda se jedná o viry, které jsou v ledvinách přítomny. U všech 4 pacientů byla virová RNA potvrzena ve všech vzorcích plic, ale ve všech vzorcích ledvin byla negativní. Ultrastrukturální vyšetření však odhalilo intracelulární vezikulární struktury podobné velikosti a morfologie v plicích s prokázanou virovou RNA a v ledvinách bez virové RNA. Ve vzorcích plic s prokázanou virovou RNA jsme pozorovali mnoho struktur, které mohly být buď virovými částicemi s typickou korónou, nebo potaženými vezikulami s elektronově hustým proteinovým pláštěm (obrázek 1a). Kromě toho jsme ve stejných vzorcích plic pozitivních na SARS-CoV-2 nalezli vakuoly, které mohly být buď membránově vázanými shluky virových částic, nebo MVB s intralumenálními vezikulami uvnitř (obrázek 1c). Na druhé straně ultrastrukturální vyšetření vzorků plic 2 pacientů bez SARS-CoV-2 (1 pitevní vzorek plic s negativní RT-PCR na virovou RNA a 1 bioptický vzorek plic před érou COVID) odhalilo stejné struktury připomínající virové částice, obalené vezikuly nebo MVB jako ve vzorku s pozitivním SARS-CoV-2 (obr. 1b a d).
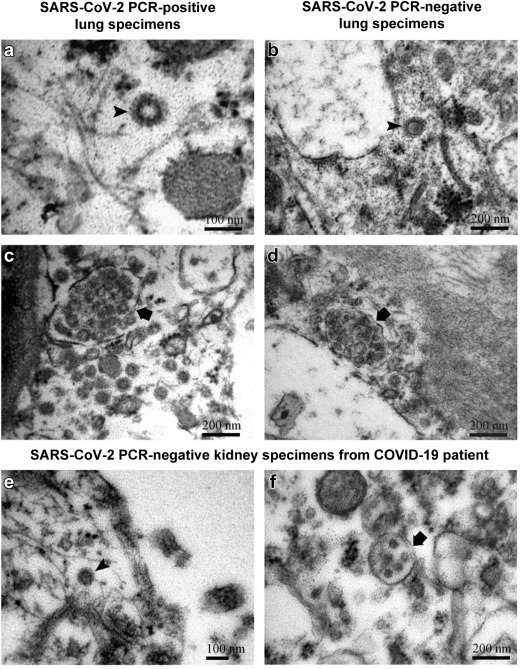
Obrázek 1 Jednotlivé vezikuly s elektronově hustým pláštěm (hrot šipky) umístěné volně v cytosolu endoteliální buňky v plicích s pozitivní reverzně transkriptázovou polymerázovou řetězovou reakcí (RT-PCR) na RNA těžkého akutního respiračního syndromu 2 (SARS-CoV-2) (a) a v plicích s negativní RT-PCR na RNA SARS-CoV-2 (b). Všimněte si podobné morfologie obou struktur na snímcích (a) a (b), které by mohly být virem nebo obaleným vezikulem. Vzhledem k výsledkům RT-PCR by pozorované struktury mohly být virem na snímku (a), ale ne na snímku (b). Vakuola s mnoha malými vezikulami uvnitř limitující membrány (šipka) v cytosolu endoteliální buňky v plicích s pozitivní RT-PCR na SARS-CoV-2 RNA (c) a v plicích s negativní RT-PCR na SARS-CoV-2 RNA (d). Všimněte si opět podobné morfologie obou struktur na snímcích (c) a (d), což by mohl být shluk virových částic nebo multivesikulární tělíska (MVB) s intralumenálními vezikulami uvnitř. Vzhledem k výsledkům RT-PCR by pozorované struktury mohly být shlukem virových částic na obrázku (c), ale ne na obrázku (d). (e,f) V cytosolu ledvinových podocytů u pacienta s pozitivním nálezem SARS-CoV-2, ale s negativní RT-PCR na SARS-CoV-2 RNA, byly pozorovány struktury připomínající viriony, obalené vezikuly nebo MVB. Vzhledem k výsledkům RT-PCR se v případě prezentovaných struktur nejedná o viry, ale o všudypřítomné obalené vezikuly a MVB.
Analýza TEM posmrtných vzorků ledvin pacientů s COVID-19 odhalila četné jednotlivé vezikuly a shluky vezikul v různých typech ledvinových buněk, a to i přes negativní RT-PCR na SARS-CoV-2 RNA (obr. 1e a f). Dále jsme provedli semikvantitativní analýzu těchto intracelulárních struktur v různých typech ledvinových buněk z 20 preimplantačních biopsií ledvin dárců před a během propuknutí SARS-CoV-2 s negativní RT-PCR na SARS-CoV-2 RNA, abychom prokázali, že tyto buněčné struktury jsou četné a všudypřítomné v různých typech buněk (tabulka 1).
Přibývá důkazů, které naznačují, že obalené vezikuly a MVB mohou napodobovat virové částice. Je však známo, že pučení obalených virů (k nimž SARS-CoV-2 patří) z plazmatické membrány nebo limitující membrány endosomu připomíná tvorbu intralumenálních vezikul uvnitř MVB. Oba procesy navíc sdílejí některé složky stejného proteinového mechanismu. V plicních endoteliálních buňkách s pozitivní RNA SARS-CoV-2 jsme skutečně detekovali intralumenální vezikuly vznikající z přerušené limitující membrány vakuoly (obrázek 1a). Toto zjištění silně naznačuje, že tato struktura není MVB, ale spíše shluk virových částic s některými z poupat virionů. Nezpochybnitelný důkaz o přítomnosti virionů by tak poskytla až imunoelektronová mikroskopie. Kromě toho by obalené vezikuly mohly také slabě připomínat virové částice, ale je třeba být opatrný ohledně intracelulárního umístění obalených vezikul. Konkrétně potahované vezikuly jsou přechodné, a proto se většinou nacházejí v těsné blízkosti membrány, z níž vznikají, protože se zbavují svého obalu během několika sekund po svém vzniku.
Závěrem lze říci, že ačkoli TEM může sloužit jako užitečná diagnostická metoda pro detekci virové infekce, je třeba být opatrný, pokud se potvrzení virové invaze opírá pouze o TEM. Pro nezpochybnitelný důkaz virové invaze do orgánů je zapotřebí dalších přesvědčivých metod, včetně imunoelektronové mikroskopie, imunohistochemie a analýzy virového genetického materiálu.”
https://www.kireports.org/article/S2468-0249(20)31368-1/fulltext
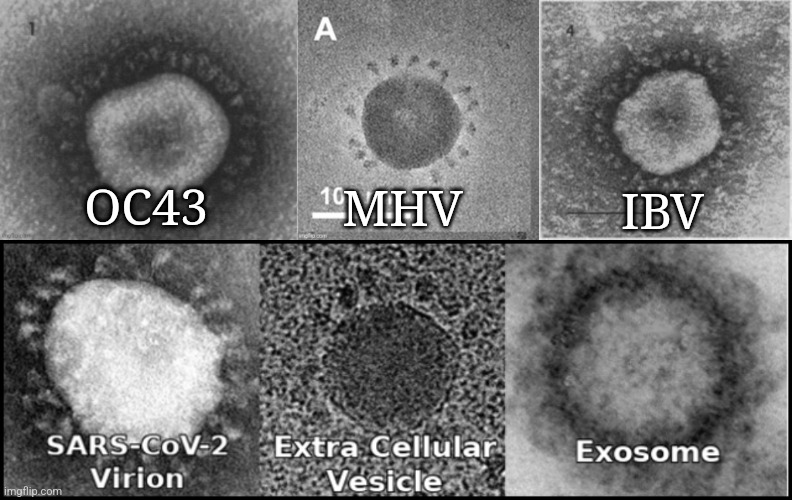
Skutečnost, že částice označované jako “SARS-COV-2” byly nalezeny nejen ve vzorcích bez “virové” RNA, ale také ve vzorcích od pacientů bez “SARS-COV-2” z doby před “Covid-19”, by měla každému intelektuálně poctivému člověku stačit k závěru, že částice na snímcích TEM nejsou ničím jiným než nesmyslným zobrazením. Připouští se, že stejné částice “SARS-COV-2” mohou být mikrovesikulární tělíska, vezikuly obalené klathrinem, Golgiho aparát, sekreční granula a vezikuly, vezikuly obalené koatomerem a/nebo exozomy. Zatímco snímky mohou být pro oko pozorovatele čímkoli, čím být nemůžou, je platný důkaz “virů”.
O něco více než rok později, v září 2021, publikovali stejní vědci další studii na téma nesprávné interpretace TEM snímků. Tentokrát sice stále uznávali, že použití TEM k identifikaci “virů” může být zavádějící a samo o sobě není vhodné jako důkaz, ale snažili se tento problém napravit pomocí vlastní metody, která byla variantou korelační mikroskopie kombinující imunohistochemické značení s TEM. Výzkumníci v podstatě použili teoretické protilátky ve snaze dokázat teoretické “viry” tvrzením, že protilátky se zaměřily na částice, které byly “SARS-COV-2”, a označily je. Tímto přístupem výzkumníci tvrdí, že dokázali rozlišit částice, které jsou “SARS-COV-2”, od částic, které nejsou “SARS-COV-2″… i když jsou tyto částice ve všech ostatních ohledech identické.
S touto teorií a nakonec i s jejich důkazy je spojeno mnoho problémů. Především, protože protilátky nebyly nikdy řádně vyčištěny ani izolovány, nelze použít jeden fiktivní výtvor k potvrzení jiného fiktivního výtvoru. I kdyby byla existence protilátek vědecky prokázána, bez vyčištění a izolace částic, o nichž se tvrdí, že jsou “SARS-COV-2”, nelze zjistit, které teoretické protilátky by byly specifické pro samotný “virus”. Bylo opakovaně prokázáno, že protilátky jsou nespecifické a mohou se vázat na mnoho jiných proteinů, než je zamýšlený cíl. Studie založené na protilátkách jsou zřídka reprodukovány, což vedlo ke krizi reprodukovatelnosti, která má za následek falešné a chybné výsledky tvořící většinu vědeckého výzkumu.
Vědci v rámci svého vlastního článku uvedli i mnoho dalších důvodů, proč jsou metody, které použili jako “důkaz”, nespolehlivé. Bylo uvedeno, že
- Imunohistochemie může být falešně pozitivní nebo negativní z několika důvodů v preanalytické nebo analytické fázi.
- Je známo, že antigeny jsou zranitelné v několika fázích imunohistochemického postupu a také během přípravy vzorků pro TEM.
- Konvenční TEM analýza je silně závislá na konzervaci tkáně, která by mohla narušit strukturu “virů”, pokud není provedena optimálně.
- Vzorek použitý pro TEM analýzu může vynechat oblast obsahující “viry”.
- Reakce IHC na úrovni světelné mikroskopie by mohla být zavádějící kvůli nesprávné interpretaci nespecifického barvení.
- Malé zvětšení a rozlišení IHC neumožňuje patologům vidět “viriony” nebo být přesvědčen, že reakce IHC kolokalizuje s “viriony”.
- I přes možnost vidět struktury (“viriony”) pomocí TEM díky jejímu vysokému rozlišení mohou být chybně interpretovány.
- Pro získání “specifické” a “spolehlivé” imunoreakce je rozhodující protokol imunoznačení, a to od prvních kroků přípravy vzorku tkáně až po volbu protilátky.
Samotný článek velmi podrobně popisuje, co se vlastně dělá při přípravě vzorků pro imunohistochemii i pro zobrazování TEM. Tyto části jsem zvýraznil, abych ukázal četné procesy a látky, kterým se vzorek pro zobrazování podrobuje. Jak zdůraznil Dr. Hillman, snímky konečného výsledku po četných úpravách provedených na vzorku lze jen stěží považovat za přesné zobrazení toho, co bylo odebráno z nitra živé bytosti.
Vědci nakonec zjistili, že pro získání požadovaných výsledků je rozhodující vhodné fixační a embedovací médium, které může omezit přístup k protilátkám i jejich kvalitu. Výsledky imunogoldového značení “SARS-CoV-2” silně závisely na volbě primární protilátky a pryskyřice, protože “specifického” barvení a uspokojivé ultrastruktury se jim podařilo dosáhnout pouze na řezech Lowicryl s “vhodnou” protilátkou. Výzkumníci vyzkoušeli různé jiné metody využívající jiné “specifické” protilátky proti SARS-COV-2 s ultratenkými řezy Epon, které všechny nepřinesly výsledky, které chtěli vidět. Je zvláštní, že na rozdíl od jejich předchozí zprávy, která skutečně obsahovala kontrolu negativních pacientů se “SARS-COV-2”, která ukázala, že stejné částice se nacházejí i u osob bez onemocnění, se výzkumníci nepokusili zjistit, zda by bylo možné získat stejné “specifické” výsledky imunoznačení pomocí vzorků od “SARS-COV-2” negativních osob.
Níže je uveden celý dokument, o kterém tvrdí, že je nezpochybnitelným důkazem toho, že “SARS-COV-2” byl nalezen v infikovaných tkáních. Na základě výše uvedeného seznamu problémů je zřejmé, že tomu tak nebylo:
Pouhé vidění nestačí k tomu, abyste uvěřili: Imunoznačení jako nezpochybnitelný důkaz přítomnosti virů SARS-CoV-2 v infikované tkáni
“Přibývá důkazů, že identifikace virionů SARS-CoV-2 transmisní elektronovou mikroskopií by mohla být zavádějící vzhledem k podobné morfologii virionů a všudypřítomným buněčným strukturám. Cílem této studie proto bylo stanovit metody pro nezpochybnitelný důkaz přítomnosti virionů SARS-CoV-2 ve sledované tkáni. Metody: Vyvinuli jsme variantu přístupu korelační mikroskopie pro identifikaci proteinů SARS-CoV-2 pomocí imunohistochemického značení proteinů SARS-CoV-2 na úrovni světelné a elektronové mikroskopie. Provedli jsme také imunogoldové značení virionů SARS-CoV-2. Výsledky: Imunohistochemické vyšetření (IHC) nukleokapsidových proteinů SARS-CoV-2 a následná korelační mikroskopie nepochybně prokázaly přítomnost SARS-CoV-2.
SARS-CoV-2 v analyzované lidské nosohltanové tkáni. Přítomnost virionů SARS-CoV-2 byla poprvé potvrzena také pomocí imunogoldového značení.
Závěry: Imunoelektronová mikroskopie je nejspolehlivější metodou pro odlišení intracelulárních virových částic od normálních buněčných struktur podobné morfologie a velikosti jako viriony. Dále jsme vyvinuli variantu korelační mikroskopie, která umožňuje patologům kontrolovat výsledky IHC provedené nejprve na rutinně používaných parafinových vzorcích, poté na semitinových a nakonec na ultratenkých řezech. Oba metodické přístupy nesporně prokázaly přítomnost virionů SARS-CoV-2 v buňkách.
1. Úvod
Od objevení viru SARS-CoV-2 bylo v mnoha studiích popsáno údajné přítomnost virionů SARS-CoV-2 ve tkáních pacientů s COVID-19 nalezených transmisní elektronovou mikroskopií (TEM) [1-3]. Jako dostatečný důkaz pro identifikaci viru se ve výše uvedených studiích používala pouze detekce virových částic pomocí TEM, což svědčí o přímé virové infekci určitých buněk a tkání. Několik autorů však upozornilo na možnou chybnou interpretaci těchto nálezů vzhledem k podobnosti struktury a velikosti virionů a normálních buněčných struktur [4,5]. V předchozí studii jsme prokázali buněčné struktury připomínající viriony SARS-CoV-2 ve vzorcích plic a ledvin SARS-CoV-2 pozitivních a negativních pacientů na základě jejich výsledků RT-PCR na SARS-CoV-2 RNA [6]. Ve světle našich výsledků jsme proto navrhli, že pro jednoznačnou identifikaci virionů v buňkách a tkáních je kromě analýzy virového genetického materiálu zapotřebí metod, jako je imunohistochemie nebo imunoelektronová mikroskopie.
Stávající metody používané pro detekci virů ve vzorcích tkání mají známá omezení. Například imunohistochemie může být falešně pozitivní nebo negativní z několika důvodů v preanalytické nebo analytické fázi. Konvenční TEM analýza navíc silně závisí na konzervaci tkáně, která může zkreslit strukturu virů, pokud není provedena optimálně. Další nevýhodou TEM analýzy je, že vzorek může vynechat oblast obsahující viry [7]. Na druhé straně je imunoelektronová mikroskopie velmi výkonnou a vysoce sofistikovanou metodou pro detekci a identifikaci virů, která je však dostupná převážně v akademickém prostředí. Metoda, která spojuje výše uvedené metody a zároveň představuje most mezi světelnou a elektronovou mikroskopií je korelační mikroskopie.
Provedli jsme variantu korelační imunohistochemie a imunogoldového značení proteinů SARS-CoV-2 pro nezpochybnitelný důkaz přítomnosti virionů SARS-CoV-2 v nosohltanové tkáni pacientů s pozitivní RT-PCR pro SARS-CoV-2 RNA. Kombinovali jsme imunohistochemické značení proteinů SARS-CoV-2 na úrovni světelné a elektronové mikroskopie, a vyvinuli tak korelační mikroskopický přístup pro SARS-CoV-2 pro identifikaci proteinů, o kterém dosud nejsou v literatuře žádné zprávy. Ukázali jsme také, že specifická a spolehlivá imunoreakce zásadně závisí na protokolu imunoznačení, od prvních kroků přípravy vzorku tkáně až po volbu protilátky. Domníváme se, že pokud je imunoznačení provedeno správně, je nejspolehlivější metodou odlišení intracelulárních virových částic od normálních buněčných struktur podobné struktury a velikosti jako viriony. Pokud je nám známo, jedná se o první zprávu o imunoznačení virionů SARS-CoV-2 na úrovni elektronové mikroskopie.
2. Materiál a metody
2.1. Pacienti
Pro imunohistochemické a imunogoldové značení virionů SARS-CoV-2 byly odebrány vzorky z pitevní tkáně nosohltanu pacientů s pozitivním výsledkem RT-PCR.
2.2. Imunohistochemie (IHC) pro korelační a transmisní elektronovou mikroskopii (TEM)
Kousky tkáně nosohltanu (5 mm3) byly fixovány ve 4% paraformaldehydu (Merck, Darmstadt, Německo) po dobu 24 hodin, dehydratovány v etanolu a zalité do parafínu. Vzorek tkáně pro imunohistochemii byl získán proděravěním parafinového bloku ručním tkáňovým děrovačem. Vypíchnuté parafinové bloky byly poté deparafinovány a rehydratovány etanolem. Získání antigenu bylo provedeno mikrovlnným ohřevem v 10 mM citrát sodném pufru, pH 6,0 (Sigma Aldrich, Burlington, MA, USA) po dobu 20 min. Endogenní peroxidázy byly blokovány 3% peroxidem vodíku (Ventana, Monterey, CA, USA) po dobu 15 min po inkubaci v primárních králičích protilátkách proti nukleokapsidovému proteinu SARS-CoV-2 (1:600; NB100, Novus Biologicals, Cambridge, UK) po dobu 2 h při pokojové teplotě. Po promytí reakčním pufrem (Ventana, Monterey, CA, USA) byl použit UltraView Universal DAB Detection Kit (Ventana, Monterey, CA, USA) s následujícím protokolem: HRP enzym konjugovaný s kozími sekundárními protilátkami proti králíkům po dobu 20 min, reakční pufr (Ventana, Monterey, CA, USA) dvakrát po dobu 5 min, směs 3,3′-diaminobenzidinu
(DAB) chromogenu a H2O2 po dobu 20 min a nakonec promytí reakčním pufrem (Ventana, Monterey, CA, USA) a destilovanou vodou po dobu 5 min.
Po IHC byly vzorky tkání přes noc převedeny do 0,1 M Millonigova fosfátového pufru a druhý den zpracovány pro transmisní elektronovou mikroskopii. Nejprve byly postfixovány v 1% OsO4 (Merck, Darmstadt, Německo) po dobu 30 min, poté byly dehydratovány v odstupňovaných koncentracích ethanolu a 1-2-propylenoxidu (Merck, Darmstadt, Německo) po dobu 10 min v každém roztoku. Poté byly kousky tkáně inkubovány ve směsi (1:1) 1-2-propylenoxidu a pryskyřice Epon 812 (Serva Electrophoresis, Heidelberg, Německo) po dobu 20 min, vloženy do 100% Eponu a polymerizovány při 60 ◦C po dobu 24 h. Následující den byly ultramikrotomem Leica EM UC6 vyříznuty semitinové řezy o velikosti 1 µm a obarveny barvicím roztokem Azure II, aby bylo možné nalézt SARS-CoV-2 pozitivní buňky jako oblast zájmu a vybrat tuto oblast pro ultratenký řez. Ultratenké řezy o velikosti 60 nm byly vyříznuty a prohlíženy v transmisním elektronovém mikroskopu JEM- 1200 EXII (JEOL, Tokio, Japonsko) při 60 kV (obrázek 1).
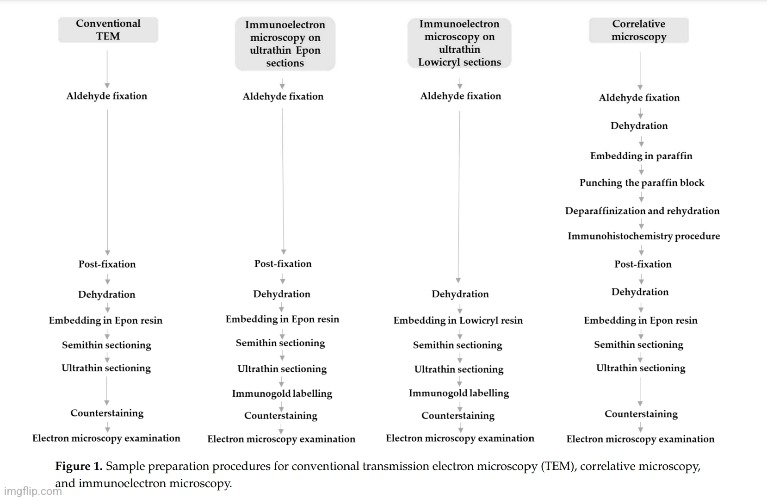
2.3. Imunogoldové značení na ultratenkých řezech
Pro imunogoldové značení na ultratenkých řezech Epon byly malé vzorky (2 mm3) tkáně nosohltanu fixovány ve směsi 4% paraformaldehydu (Merck, Darmstadt, Německo) a 2% glutaraldehydu (Serva, Heidelberg, Německo) v 0,2 M kakodylátovém pufru (pH 7,3) po dobu 3 hodin při 4 ◦C. Po nočním opláchnutí v 0,33 M sacharóze v 0,2 M kakodylátovém pufru následovala postfixace 1% OsO4 (Serva, Heidelberg, Německo) po dobu 1 h. Po opláchnutí v 0,33 M sacharóze v 0,2 M kakodylátovém pufru následovala postfixace 1% OsO4.
dehydrataci v ethanolu byly vzorky tkáně zalité do pryskyřice Epon 812 (Serva Electrophoresis, Heidelberg, Německo) a rozřezány na ultratenké řezy (60 nm silné), které byly odebrány na niklové mřížky. Úprava pro demaskování antigenu byla provedena inkubací některých mřížek ve vlhké komoře na velké kapce nasyceného vodného roztoku meta-periodátu sodného (Merck, Darmstadt, Německo) po dobu 1 h při pokojové teplotě. Mřížky byly poté promyty v destilované vodě. Nespecifické značení bylo blokováno blokovacím pufrem (5% fetální telecí sérum v 0,1% BSA v PBS (promývací pufr)) po dobu 30 min při pokojové teplotě. Byly použity primární protilátky proti nukleokapsidovému proteinu SARS-CoV-2 (NB100; Novus Biologicals, Cambridge, UK) zředěné v poměru 1:50 nebo proti hrotovému glykoproteinu S1 SARS-CoV-2 (ab 275759; Abcam, Cambridge, UK) zředěné v poměru 1:100 a inkubovány přes noc při 4 ◦C. Po promytí v promývacím pufru byly aplikovány kozí protilátky proti králíkovi s 18 nm zlatem (Au) ředěné 1:40 v blokovacím pufru po dobu 90 min. Ve všech případech výrobci použitých protilátek poskytli doklad o ověření technických specifikací. Ve všech případech byly provedeny také negativní kontroly, při nichž byly primární protilátky nahrazeny PBS. Řezy byly barveny protibarvením uranylacetátem a citrátem olovnatým.
Pro imunogoldové značení na ultratenkých řezech Lowicryl byly malé kostky (1 mm 3) tkáně nosohltanu přeneseny do 2% paraformaldehydu (Merck, Darmstadt, Německo) plus 0,05% glutaraldehydu (Serva, Heidelberg, Německo) v PBS na 1 hodinu při pokojové teplotě. Vzorky byly dehydratovány postupným snižováním teploty a poté vloženy do pryskyřice Lowicryl HM20 (Polysciences, Eppelheim, Německo) v přístroji Leica AFS (Leica Microsystems, Vídeň, Rakousko) podle následujícího protokolu: 30 % ethanol po dobu 30 min při 0 ◦C, 55 % ethanol po dobu 30 min při -15 ◦C, 70 % ethanol po dobu 30 min při -30 ◦C, 100 % ethanol po dobu 1 h při -50 ◦C, 75% ethanol/25% HM20 po dobu 1 h při -50 ◦C, 50% ethanol/50% HM20 po dobu 1 h při -50 ◦C, 25% ethanol/75% HM20 po dobu 1 h při -50 ◦C, 100% HM20 po dobu 1 h a 100% HM20 přes noc při -50 ◦C. HM20 byl polymerován 48 h při -50 ◦C a poté 24 h při -20 ◦C pod UV světlem. Byly vyříznuty ultratenké řezy (tloušťka 60 nm) a odebrány na niklové mřížky. Řezy byly promyty v promývacím pufru (0,1% Na-azid, 0,8% BSA a 0,1% IGSS želatina v PBS), blokovány v blokovacím pufru (5% fetální telecí sérum v 0. 1% BSA v PBS (promývací pufr)) po dobu 30 minut při pokojové teplotě a inkubovány přes noc při 4 ◦C s primárními protilátkami proti nukleokapsidovému proteinu SARS-CoV-2 (NB100-56576; Novus Biologicals, Cambridge, UK) zředěnými v poměru 1:50 nebo proti hrotovému glykoproteinu S1 SARS-CoV-2 (ab 275759; Abcam, Cambridge, UK) zředěným v poměru 1:100. Po promytí v promývacím pufru byly aplikovány kozí protilátky proti králíkům se sekundárním zlatem 18 nm (Au) ředěné 1:40 v blokovacím pufru po dobu 90 min. Řezy byly protibarveny uranylacetátem a citrátem olovnatým. Ultratenké řezy byly pozorovány v transmisním elektronovém mikroskopu Philips CM100 (Philips, Amsterdam, Nizozemsko) při 80 kV (obrázek 1).
3. Výsledky
3.1. Korelační mikroskopický přístup a detekce viru SARS-CoV-2
Výsledky imunohistochemie nukleokapsidových proteinů SARS-CoV-2 a následné korelační mikroskopie nepochybně prokázaly přítomnost virionů SARS-CoV-2 v analyzované lidské nosohltanové tkáni (obrázek 2). Zjistili jsme buňky s pozitivním
imunohistochemickým barvením v semitinových řezech světelnou mikroskopií (obrázek 2a). Stejné buňky s pozitivním imunohistochemickým barvením byly vyšetřeny na ultratenkých řezech Epon, které vykazovaly elektronově hustý materiál v cytoplazmě uvnitř endozomů (obrázek 2b,c). Nakonec jsme při větším zvětšení identifikovali v endozomech sledovaných buněk viriony označené jemnou zrnitou elektronově hustou reakcí odpovídající produktu DAB (obrázek 2d).
3.2. Přístup k imunoelektronové mikroskopii a detekce virů SARS-CoV-2
Pomocí imunogoldového značení jsme potvrdili přítomnost virionů SARS-CoV-2 ve vzorcích lidské nazofaryngeální tkáně. Výsledky této metody značně závisely na typu ultratenkých řezů a primárních protilátek použitých v protokolu imunoznačení (obr. 3). Imunogoldová reakce na ultratenkých řezech Epon s primárními protilátkami proti nukleokapsidovému proteinu SARS-CoV-2 (Novus Biologicals) byla všudypřítomná, a tudíž nespecifická (obrázek 3a), zatímco na ultratenkých řezech Epon s primárními protilátkami proti hrotovému glykoproteinu S1 SARS-CoV-2 (Abcam) byla řídká a nespecifická (obrázek 3b). Po postupu demaskování antigenu na ultratenkých řezech Epon (popsaném v metodách) s primárními protilátkami proti hrotovému glykoproteinu S1 SARS-CoV-2 (Abcam) bylo imunogoldové značení specifičtější, ale slabé (obrázek 3c). Imunogoldové značení na ultratenkých řezech Lowicryl s primárními protilátkami proti SARS-CoV-2 spike glykoproteinu S1 (Abcam) bylo specifické a intenzivní (obrázek 3d).
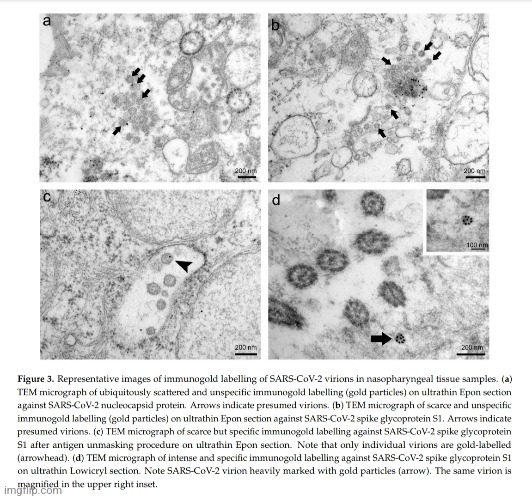
4. Diskuse
Analýza virového genetického materiálu z nosohltanové tkáně pacientů sama o sobě není dostatečným důkazem aktivní infekce v tělesných tkáních virem SARS-CoV-2, ale pozitivní test RT-PCR, který je v současné době zavedeným testem na infekci SARS-CoV-2, je předpokladem pro další analýzu přítomnosti viru SARS-CoV-2 v konkrétní tkáni. Stejně tak analýza TEM sama o sobě nestačí k jednoznačnému průkazu přítomnosti virionů SARS-CoV-2 v zájmové tkáni vzhledem k podobné struktuře a velikosti těchto virionů a všudypřítomným buněčným strukturám [4,5]. V předchozí studii jsme proto zdůraznili, že po pozitivním testu RT-PCR na RNA SARS-CoV-2 je pro spolehlivou identifikaci virionů v podezřelých infikovaných tkáních nutná IHC nebo dokonce imunoelektronová mikroskopie.
V této studii uvádíme dva přístupy k imunoznačení vzorků nasofaryngeální tkáně z pitvy pacientů s pozitivním výsledkem RT-PCR na SARS-CoV-2 RNA. Provedli jsme tedy korelační mikroskopii, při níž jsme spojili výhody IHC a elektronové mikroskopie k analýze téhož vzorku. Nejprve jsme provedli imunohistochemickou reakci proti nukleokapsidovému proteinu SARS-CoV-2 s diaminobenzidinovým (DAB) chromogenem na parafinových řezech, což je standardní diagnostická metoda v naší patologické laboratoři. DAB se oxiduje v přítomnosti peroxidázy a peroxidu vodíku, poté se váže na sekundární protilátky, což vede k usazování hnědě zbarveného precipitátu v místě enzymatické aktivity, viditelného při světelné mikroskopii a také při elektronové mikroskopii, zejména po postfixaci osmiem [8]. Stejný imunohistochemický protokol jsme provedli také na deparafinovaných malých kouscích tkáně, které jsme následně fixovali v osmiu, vložili do Eponové pryskyřice a rozřezali na semitinové řezy. Nakonec byla vybraná oblast buněk s pozitivním imunohistochemickým barvením rozřezána pro TEM. Imunohistochemická reakce umožnila vizualizaci imunohistochemicky značených virionů SARS-CoV-2 v infikovaných buňkách na semitinovém řezu světelnou mikroskopií, po níž následovala detekce virionů SARS-CoV-2 v TEM ve stejné buňce na ultratenkých řezech. Podařilo se nám zachovat imunohistochemické značení virionů pomocí DAB během postupu zakládání do TEM a ukázali jsme, že IHC a TEM lze použít jako analytické metody pro jednoznačnou identifikaci virionů SARS-CoV-2.
Imunohistochemie je běžnou doplňkovou metodou v patologii pro diagnostické účely, ale všechny kroky této techniky musí být optimalizovány. Je známo, že antigeny jsou zranitelné v několika fázích imunohistochemického postupu a také během přípravy vzorků pro TEM [9,10]. Pečlivým výběrem protokolů pro postup IHC a TEM a precizním provedením všech postupů jsme zachovali dobrou dostupnost epitopů a dosáhli jsme také vysoce specifické reakce na úrovni elektronové mikroskopie.
Z našeho pohledu je imunoelektronová mikroskopie nejspolehlivější metodou pro odlišení intracelulárních virových částic od normálních buněčných struktur podobné morfologie a velikosti jako viriony. Bohužel je k této metodice zapotřebí speciální a drahé vybavení. Proto jsme vyvinuli variantu korelační mikroskopie, která umožňuje každé rutinní patologické laboratoři kontrolovat její výsledky IHC prováděné na rutinně používaných parafinových vzorcích, stejně jako pomocí transmisního elektronového mikroskopu bez vysoce vyvinutých přístrojů a sofistikovaných technik. Konkrétně reakce IHC na úrovni světelné mikroskopie jako takové by mohla být zavádějící v důsledku různých faktorů v preanalytické fázi a chybné interpretace nespecifického barvení. Navíc malé zvětšení a rozlišení IHC neumožňuje patologům vidět viriony nebo být přesvědčen, že reakce IHC kolokalizuje s viriony. Stejně tak konvenční analýza TEM sama o sobě také nestačí k nepochybnému důkazu přítomnosti virionů. Totiž i přes možnost vidět struktury (viriony) pomocí TEM díky jejímu vysokému rozlišení je můžeme chybně interpretovat. Proto je možné použít pouze kombinaci lokalizace pozitivní imunoreakce na viru (tj. viry) a současné identifikace této struktury na ultrastrukturální úrovni poskytuje nezpochybnitelný důkaz přítomnosti virionů. Patologům v rutinních patologických laboratořích bychom proto mohli doporučit, aby si výsledky IHC proti viru SARS-CoV-2 potvrdili korelační mikroskopií popsanou v našem rukopise. To je podle našeho názoru hlavní vědecký výstup naší práce, který lze přenést do každodenní praxe. Jsme si vědomi, že představuje jen malý kousek skládačky SARS-CoV-2, nicméně každý kousek je důležitý pro zpřehlednění celého obrazu. V dnešní době si nemůžeme dovolit falešně pozitivní nebo falešně negativní patologické zprávy, zejména pokud máme odpovídající znalosti a metodiku.
Abychom se vyhnuli úskalím při imunogoldovém značení, jsou zásadní vhodná fixační a embedovací média, která mohou omezit přístup k protilátkám i jejich kvalitu [11,12]. V naší studii výsledky imunogoldového značení virionů SARS-CoV-2 silně závisely na výběru primární protilátky a pryskyřice. Pouze na Lowicrylových řezech a s vhodnou protilátkou jsme byli schopni získat specifické barvení a uspokojivou ultrastrukturu. Imunogoldové značení koronavirů již bylo popsáno [13], ale domníváme se, že toto je dosud první zpráva o identifikaci virionů SARS-CoV-2 pomocí imunoelektronové mikroskopie.
5. Závěry
Závěrem lze říci, že imunoelektronová mikroskopie, pokud je provedena správně, je nejspolehlivější metodou pro odlišení intracelulárních virových částic od normálních buněčných struktur podobné morfologie a velikosti jako viriony. Navíc jsme vyvinuli variantu korelační mikroskopie, která umožňuje patologům kontrolovat výsledky IHC provedené nejprve na rutinně používaných parafinových vzorcích, poté na semitinových a nakonec na ultratinových řezech bez použití vysoce vyvinutých přístrojů a sofistikovaných technik. Obě metody prokázaly, že teprve kolokalizace pozitivní imunoreakce na zájmové struktuře (tj. virech) a identifikace této struktury na ultrastrukturální úrovni poskytuje nezpochybnitelný důkaz přítomnosti virionů.”
https://www.ncbi.nlm.nih.gov/labs/pmc/articles/PMC8473209/
Shrnutí:
- Dr. Harold Hillman si položil otázku: “Kolik toho snímek pořízený tímto přístrojem vypovídá o struktuře živé buňky?”.
- TEM umožňuje mnohem větší rozlišení a zvětšení než světelný mikroskop, ale tkáň nemůže přežít nízký tlak, bombardování elektrony a rentgenové záření v elektronovém mikroskopu
- Proto musí být tkáň potažena nánosem solí osmia olova nebo wolframu, který se těmito činidly neničí, a proto může být zkoumán
- Když se podíváme na ilustraci elektronového mikrofotografu:
- Zvíře bylo usmrceno
- Ochladí se
- jeho tkáň je vyříznuta
- Tkáň je fixována (usmrcena)
- Je obarvena solí těžkého kovu
- je dehydratována zvyšující se koncentrací alkoholu
- Smršťuje se
- Alkohol se extrahuje tukovým rozpouštědlem, propylenoxidem.
- Ten je nahrazen epoxidovou pryskyřicí
- Za několik dní ztvrdne
- Řežou se úseky o tloušťce jedné desetiny milimetru nebo menší.
- Vloží se do elektronového mikroskopu, z něhož se odčerpá téměř všechen vzduch.
- Je na něj namířen svazek elektronů o napětí 10 000 až 3 000 000 voltů.
- Některé elektrony dopadají na fosforeskující stínítko.
- Elektronoví mikroskopisté zvolí pole a zvětšení, které zobrazí znaky, jež chtějí demonstrovat.
- Obraz může být zvětšen
- Pořizují se fotografie a některé se vyberou jako důkazní materiál
- Okamžitě je vidět, jakou cestu urazila tkáň od života k ilustraci v knize.
- Většina nových struktur v buňkách patrných při elektronové mikroskopii jsou artefakty

- Mnoho studií uvádí detekci údajných “virových” částic transmisní elektronovou mikroskopií (TEM), která byla použita jako dostatečný důkaz “virové” invaze do ledvinové tkáně, ale chyběly údaje týkající se detekce “virové” RNA nebo jiných cenných metod pro detekci “virů” ve vzorcích ledvin
- V jedné studii prezentované částice ve výše uvedených studiích vykazují průměr 50 až 150 nm a elektronově hustý plášť podobný koruně, takže se mohou jevit jako podobné “koronavirům”, ale také jako podobné všudypřítomným obaleným vezikulám, jako jsou vezikuly obalené klathrinem nebo vezikuly obalené COPI nebo COPII
- Shluky “virových” částic uvnitř vakuoly se navíc mohou podobat multivesikulárním tělískům (MVB), což jsou pravidelné struktury endocytární dráhy
- Ve studii 4 pacientů s potvrzeným “SARS-COV-2” byla “virová” RNA potvrzena ve všech vzorcích plic, ale byla negativní ve všech vzorcích ledvin.
- Ultrastrukturální vyšetření však odhalilo intracelulární vezikulární struktury podobné velikosti a morfologie v plicích s prokázanou “virovou” RNA a v ledvinách bez “virové” RNA
- Ve vzorcích plic s prokázanou “virovou” RNA autoři pozorovali mnoho struktur, které mohly být buď “virovými” částicemi s typickou korunkou, nebo potaženými vezikulami s elektronově hustým proteinovým obalem
- Kromě toho ve stejných “SARS-CoV-2 pozitivních” plicních vzorcích nalezli vakuoly, které by mohly být buď membránově vázanými shluky “virových” částic, nebo MVB s intralumenálními vezikulami uvnitř.
- Na druhé straně ultrastrukturální vyšetření vzorků plic 2 pacientů bez “SARS-CoV-2” (1 pitevní vzorek plic s negativní RT-PCR na “virovou” RNA a 1 bioptický vzorek plic před érou “COVID”) odhalilo stejné struktury připomínající “virové” částice, obalené vezikuly nebo MVB jako ve vzorku s pozitivním “SARS-CoV-2”.
- TEM analýza vzorků ledvin post mortem pacientů s “COVID-19” odhalila četné jednotlivé vezikuly a shluky vezikul v různých typech ledvinových buněk, a to i přes negativní RT-PCR na RNA “SARS-CoV-2”.
- Dále provedli semikvantitativní analýzu těchto intracelulárních struktur v různých typech ledvinových buněk z 20 preimplantačních biopsií ledvin dárců před a během propuknutí nemoci “SARS-CoV-2”, při negativní RT-PCR na RNA “SARS-CoV-2”, aby prokázali, že tyto buněčné struktury jsou četné a všudypřítomné v různých typech buněk.
- Přibývá důkazů, které naznačují, že obalené vezikuly a MVB mohou napodobovat “virové” částice.
- Je známo, že vylučování obalených “virů” (k nimž patří “SARS-CoV-2”) z plazmatické membrány nebo hraniční membrány endosomu se podobá tvorbě intralumenálních vezikul uvnitř MVB.
- Kromě toho mohou obalené vezikuly také slabě připomínat “virové” částice
- Autoři uzavírají, že ačkoli TEM může sloužit jako užitečná diagnostická metoda pro detekci “virové” infekce, je třeba být opatrný, pokud se potvrzení “virové” invaze opírá pouze o TEM
- Pro nezpochybnitelný důkaz “virové” invaze do orgánů je třeba dalších přesvědčivých metod, včetně imunoelektronové mikroskopie, imunohistochemie a analýzy “virového” genetického materiálu.

- Přibývá důkazů, že identifikace “virionů SARS-CoV-2” transmisní elektronovou mikroskopií by mohla být zavádějící vzhledem k podobné morfologii “virionů” a všudypřítomných buněčných struktur.
- Podle autorů je imunoelektronová mikroskopie nejspolehlivější metodou pro odlišení intracelulárních “virových” částic od normálních buněčných struktur podobné morfologie a velikosti jako “viriony”
- Několik výzkumníků upozornilo na možnou chybnou interpretaci nálezů TEM “SARS-COV-2” kvůli podobnosti struktury a velikosti “virionů” a normálních buněčných struktur
- V předchozí studii autoři uvádějí, že na základě výsledků RT-PCR na RNA “SARS-CoV-2” prokázali v plicních a ledvinových vzorcích pozitivních a negativních pacientů “SARS-CoV-2” buněčné struktury připomínající “viriony SARS-CoV-2”.
- Stávající metody používané k detekci “virů” ve vzorcích tkání mají známá omezení.
- Imunohistochemie může být falešně pozitivní nebo negativní z několika důvodů v preanalytické nebo analytické fázi
- konvenční TEM analýza je silně závislá na konzervaci tkáně, která může zkreslit strukturu “virů“, pokud není provedena optimálně
- Další nevýhodou TEM analýzy je, že vzorek může vynechat oblast obsahující “viry”.
- Autoři provedli variantu korelační imunohistochemie a imunogoldového značení proteinů “SARS-CoV-2” pro nezpochybnitelný důkaz přítomnosti “virionů SARS-CoV-2” v nosohltanové tkáni pacientů s pozitivní RT-PCR na RNA “SARS-CoV-2” (všimněte si, že nezmínili žádné kontroly s použitím NP tkáně od “SARS-COV-2” negativních pacientů).
- Tvrdili, že prokázali, že specifická a spolehlivá imunoreakce rozhodujícím způsobem závisí na protokolu imunoznačení, od prvních kroků přípravy vzorku tkáně až po výběr protilátky.
- Přiložil jsem náčrt jednotlivých procesů, kterými vzorky procházejí, abyste viděli, kolika látkám jsou vystaveny a kolika změnami procházejí
- Proces imunohistochemie:
- Kousky tkáně nosohltanu byly fixovány ve 4% paraformaldehydu po dobu 24 hodin, dehydratovány v ethanolu a vloženy do parafínu.
- Vzorek tkáně pro imunohistochemii byl získán proděravěním parafinového bloku ručním tkáňovým děrovačem.
- Vypíchnuté parafinové bloky byly poté deparafinovány a rehydratovány etanolem.
- Získání antigenu bylo provedeno mikrovlnným ohřevem v 10 mM citrát sodném pufru, pH 6,0 po dobu 20 min.
- Endogenní peroxidázy byly blokovány 3% peroxidem vodíku po dobu 15 min po inkubaci s primárními králičími protilátkami proti nukleokapsidovému proteinu “SARS-CoV-2” po dobu 2 h při pokojové teplotě.
- Po promytí reakčním pufrem byl použit UltraView Universal DAB Detection Kit s následujícím protokolem:
- HRP enzym konjugovaný s kozími sekundárními protilátkami proti králíkům po dobu 20 min.
- Reakční pufr dvakrát po dobu 5 min
- Směs chromogenu 3,3′-diaminobenzidinu (DAB) a H2O2 po dobu 20 min.
- Promývání reakčním pufrem a destilovanou vodou po dobu 5 min.
- Proces transmisního elektronového mikroskopu:
- Po IHC byly vzorky tkáně přes noc přeneseny do 0,1 M Millonigova fosfátového pufru.
- Nejprve byly postfixovány v 1% OsO4 po dobu 30 min.
- Byly dehydratovány v odstupňovaných koncentracích ethanolu a oxidu propylénového 1-2-propylénoxidu po dobu 10 min v každém roztoku.
- Kousky tkáně byly poté inkubovány ve směsi (1:1) 1-2-propylenoxidu a pryskyřice Epon 812 po dobu 20 min.
- Byly vloženy do 100% Eponu
- poté polymerizovány při 60 ◦C po dobu 24 h
- Následující den byly ultramikrotomem Leica EM UC6 vyříznuty polotvaré řezy o velikosti 1 µm a obarveny barvicím roztokem Azure II, aby se našly “SARS-CoV-2 pozitivní” buňky jako oblast zájmu a aby se tato oblast vybrala pro ultratenký řez.
- Ultratenké řezy o velikosti 60 nm byly vyříznuty a prohlédnuty v transmisním elektronovém mikroskopu.
- Postup značení imunogoldem na ultratenkých řezech (řezy Epon):
- Malé vzorky (2 mm3) tkáně nosohltanu byly fixovány ve směsi 4% paraformaldehydu a 2% glutaraldehydu v 0,2 M kakodylátovém pufru (pH 7,3) po dobu 3 h při 4 ◦C.
- Po nočním opláchnutí v 0,33 M sacharóze v 0,2 M kakodylátovém pufru následovala postfixace 1% OsO4 po dobu 1 h.
- Po dehydrataci v ethanolu byly vzorky tkáně vloženy do pryskyřice Epon 812 a rozřezány na ultratenké řezy (60 nm silné), které byly odebrány na niklové mřížky.
- Úprava pro odmaskování antigenu byla provedena inkubací některých mřížek ve vlhké komoře na velké kapce nasyceného vodného roztoku meta-periodátu sodného po dobu 1 h při pokojové teplotě.
- Mřížky byly poté promyty v destilované vodě.
- Nespecifické značení bylo blokováno blokovacím pufrem (5% fetální telecí sérum v 0,1% BSA v PBS (promývací pufr)) po dobu 30 min při pokojové teplotě.
- Primární protilátky proti nukleokapsidovému proteinu “SARS-CoV-2” nebo proti hrotovému glykoproteinu “SARS-CoV-2” S1 zředěné v poměru 1:100 byly použity a inkubovány přes noc při 4 ◦C.
- Po promytí v promývacím pufru byly aplikovány sekundární kozí protilátky proti králíkům s 18 nm zlatem (Au) ředěné 1:40 v blokovacím pufru po dobu 90 min.
- Ve všech případech byly provedeny také negativní kontroly, v nichž byly primární protilátky nahrazeny PBS.
- Řezy byly protibarveny uranylacetátem a citrátem olovnatým.
- Postup značení imunogoldem na ultratenkých řezech (Lowicryl sections):
- Malé kostky (1 mm 3) nazofaryngeální tkáně byly přeneseny do 2% paraformaldehydu plus 0,05% glutaraldehydu v PBS na 1 hodinu při pokojové teplotě.
- Vzorky byly dehydratovány postupným snižováním teploty.
- vloženy do pryskyřice Lowicryl HM20 v přístroji Leica AFS podle následujícího protokolu:
- 30% ethanol po dobu 30 min při teplotě 0 ◦C
- 55% ethanol po dobu 30 min při -15 ◦C
- 70% ethanol po dobu 30 min při -30 ◦C
- 100% ethanol po dobu 1 h při -50 ◦C
- 75% ethanol/25% HM20 po dobu 1 h při -50 ◦C
- 50% ethanol/50% HM20 po dobu 1 h při -50 ◦C
- 25% ethanol/75% HM20 po dobu 1 h při -50 ◦C
- 100% HM20 po dobu 1 h a 100% HM20 přes noc při -50 ◦C
- HM20 byl polymerován 48 h při -50 ◦C a poté 24 h při -20 ◦C pod UV světlem.
- Ultratenké řezy (tloušťka 60 nm) byly vyříznuty a odebrány na niklové mřížky.
- Řezy byly promyty v promývacím pufru (0,1% Na-azid, 0,8% BSA a 0,1% IGSS želatina v PBS).
- blokovány v blokovacím pufru (5% fetální telecí sérum v 0,1% BSA v PBS (promývací pufr)) po dobu 30 minut při pokojové teplotě.
- Inkubováno přes noc při 4 ◦C s primárními protilátkami proti nukleokapsidovému proteinu “SARS-CoV-2” zředěnými v poměru 1:50 nebo proti hrotovému glykoproteinu S1 “SARS-CoV-2” zředěnými v poměru 1:100.
- Po promytí v promývacím pufru byly aplikovány kozí sekundární protilátky proti králíkům s 18 nm zlatem (Au) ředěné 1:40 v blokovacím pufru po dobu 90 min.
- Řezy byly kontrastně obarveny uranylacetátem a citrátem olovnatým.
- Autoři uvádějí, že pomocí imunogoldového značení potvrdili přítomnost “virionů SARS-CoV-2” ve vzorcích lidské nazofaryngeální tkáně.
- Výsledky této metody však značně závisely na typu ultratenkých řezů a primárních protilátek použitých v protokolu imunoznačení.
- Imunogoldová reakce na ultratenkých řezech Epon s primárními protilátkami proti nukleokapsidovému proteinu “SARS-CoV-2” byla všudypřítomná, a proto nespecifická.
- Na ultratenkých Eponových řezech s primárními protilátkami proti hrotovému glykoproteinu S1 viru SARS-CoV-2 byla řídká a nespecifická.
- Po postupu demaskování antigenu na ultratenkých řezech Epon s primárními protilátkami proti hrotovému glykoproteinu S1 viru SARS-CoV-2 bylo imunogoldové značení “specifičtější”, ale slabé.
- Teprve když provedli imunogoldové značení na ultratenkých řezech Lowicryl s primárními protilátkami proti hrotovému glykoproteinu S1 “SARS-CoV-2”, byla jejich reakce “specifická” a intenzivní
- Analýza “virového” genetického materiálu nosohltanové tkáně pacientů sama o sobě není dostatečným důkazem aktivní infekce “SARS-CoV-2” v tělesných tkáních, ale pozitivní test RT-PCR je předpokladem pro další analýzu přítomnosti viru “SARS-CoV-2” v konkrétní tkáni.
- analýza TEM sama o sobě nestačí k jednoznačnému důkazu přítomnosti virionů “SARS-CoV-2” v zájmové tkáni vzhledem k podobné struktuře a velikosti těchto “virionů” a všudypřítomných buněčných struktur.
- Protože tyto kroky samy o sobě nejsou platným důkazem, provedli autoři korelační mikroskopii, při níž spojili výhody IHC a elektronové mikroskopie k analýze téhož preparátu
- Imunohistochemie je běžnou doplňkovou metodou v patologii pro diagnostické účely, ale všechny kroky této techniky musí být optimalizovány
- Je známo, že antigeny jsou zranitelné v několika fázích imunohistochemického postupu a také během přípravy vzorku pro TEM.
- Z jejich hlediska je imunoelektronová mikroskopie nejspolehlivější metodou pro rozlišení intracelulárních “virových” částic od normálních buněčných struktur podobné morfologie a velikosti jako “viriony”
- Autoři však připouštějí, že reakce IHC na úrovni světelné mikroskopie jako takové může být zavádějící v důsledku různých faktorů v preanalytické fázi a chybné interpretace nespecifického barvení
- Navíc malé zvětšení a rozlišení IHC neumožňuje patologům vidět “viriony” nebo být přesvědčen, že reakce IHC kolokalizuje s “viriony”.
- Podobně konvenční analýza TEM sama o sobě také nestačí k nepochybnému důkazu přítomnosti “virionů”.
- Konkrétně, i přes možnost vidět struktury (“viriony”) pomocí TEM díky jejímu vysokému rozlišení, mohou být chybně interpretovány.
- Pouze kombinace lokalizace pozitivní imunoreakce na zájmovou strukturu (tj. “viry”) a současné identifikace této struktury na ultrastrukturální úrovni poskytuje nezpochybnitelný důkaz přítomnosti “virionů”.
- Jinými slovy, autoři se domnívají, že kombinace dvou technik, které, jak sami připouštějí, nelze považovat za důkaz, je nějakým způsobem považována za důkaz
- Aby se předešlo úskalím při imunogoldovém značení, je rozhodující vhodné fixační a embedovací médium, které může omezit přístup k protilátkám i jejich kvalitu.
- V jejich studii výsledky imunogoldového značení “virionů SARS-CoV-2” silně závisely na výběru primární protilátky a pryskyřice.
- Pouze na řezech z Lowicrylu a s vhodnou protilátkou se jim podařilo získat “specifické” barvení a uspokojivou ultrastrukturu
- Autoři dospěli k závěru, že imunoelektronová mikroskopie, pokud je provedena správně, je nejspolehlivější metodou pro rozlišení intracelulárních “virových” částic od normálních buněčných struktur podobné morfologie a velikosti jako “viriony”

Co přesně jsou částice, které byly vybrány z moře miliard podobných částic, aby byly použity jako reprezentace “SARS-COV-2”? Jsou to obalené vezikuly, multivesikulární tělíska, exozomy, Golgiho tělíska a kostomery obalené vezikuly, sekreční vezikuly a/nebo vezikuly obalené klathrinem? Jsou to všechny nebo žádná z výše uvedených možností? Jsou to prostě artefakty, které vznikají v důsledku četných procesů měnících strukturu, jimiž vzorky procházejí, aby bylo možné získat snímky, jak ukázal Dr. Harold Hillman ve svém nedoceněném výzkumu?
Ať už se jedná o cokoli, je naprosto nemožné tvrdit, že tyto částice jsou “SARS-COV-2” nebo jakýkoli jiný “virus”, protože nikdy nebyly řádně vyčištěny ani izolovány přímo ze vzorků nemocných lidí. Právě z tohoto důvodu nemohou výzkumníci odlišit částice, o nichž se domnívají, že jsou “SARS-COV-2”, od jakýchkoli jiných stejných nebo téměř stejných normálních “nevirových” částic ve vzorku. Nikdy neměli přesně ty částice, o kterých tvrdí, že jsou “SARS-COV-2”, oddělené a osvobozené od všeho ostatního (tj. izolované). Absolutní izolace je jediný způsob, jak si může být každý výzkumník zcela jistý, že částice, se kterými pracuje, jsou ty, které považuje za příčinu onemocnění. Je to jediný způsob, jak mohou prokázat patogenitu při dodržení vědecké metody. Je to jediný způsob, jak mohou částice biochemicky a molekulárně charakterizovat. Je to jediný způsob, jak se mohou pokusit prokázat specifičnost určitých protilátek. Jedině tak mohou mít snímky TEM vůbec nějakou hodnotu jako důkaz “virových” částic.
Bez purifikace a izolace částic považovaných za “SARS-COV-2” získáme matoucí, falešné a chybné výsledky. Jedna skupina výzkumníků tvrdí, že částice “korony” jsou novým “virem”, zatímco jiná skupina výzkumníků tvrdí, že jde o multivesikulární tělíska a/nebo jiné normální subcelulární částice. Dostáváme výsledky nespecifických protilátek, o kterých se tvrdí, že jsou specifické, ale jejich specifičnost nejsou nezávislí výzkumníci schopni prokázat a reprodukovat. Částice “SARS-COV-2” se nacházejí ve vzorcích s potvrzenou “virovou” RNA i ve vzorcích bez jakékoli “virové” RNA. A co je nejdůležitější, částice “SARS-COV-2” se nacházejí ve vzorcích od PCR negativních pacientů odebraných ještě předtím, než se začalo mluvit o existenci “viru”.
Když si to všechno dáme dohromady, je naprosto jasné, že snímky částic, o kterých se tvrdí, že jsou “SARS-COV-2”, jsou stejně nesmyslné jako výsledky “virového” genetického materiálu získaného pomocí PCR. Jsou stejně nesmyslné jako “specifické” protilátky, které se pravidelně vážou na necílový materiál. Jsou stejně bezvýznamné jako počítačem vytvořené sešité genomy z nečištěných zdrojů. Ve všech měřitelných ohledech jsou nepřímé výsledky, které údajně identifikují “virové” entity, jejichž existence nebyla nikdy prokázána v purifikovaném a izolovaném stavu, naprosto nesmyslné. Tyto vylepšené obrazy nespecifických částic mají hodnotu pouze pro ty, kteří vás zmanipulovali prostřednictvím strachu a propagandy. Nedovolte jim, aby nad vámi měli do budoucna jakoukoli další moc.
Až najdou úplně stejné “virové” částice u těch, o nichž se říká, že “virus” nemají, je čas, aby virologie přiznala to, co je zřejmé:

